
外泌体-中性粒细胞耦合策略介导的肿瘤抗转移治疗研究
癌转移是导致恶性肿瘤患者死亡的主要原因之一,也是当前肿瘤治疗中最难以有效干预的环节。越来越多证据表明,肿瘤来源外泌体(tumor‑derived exosomes, TDEs)在转移发生发展中发挥关键作用:TDEs 可携带细胞因子、核酸、脂质等肿瘤特异性生物分子,经外周血循环到达远端器官并诱导前转移微环境形成,从而促进肿瘤细胞定植与转移扩增。因此,在血管系统中“在途拦截”并清除TDEs,被认为是一条极具潜力的抗转移策略。然而,现有针对外泌体的清除或阻断手段在体内循环环境中往往面临靶向效率不足、作用持续性有限以及难以实现高效特异捕获/灭活等瓶颈,导致整体疗效受限。另一方面,中性粒细胞作为外周血中重要的先天免疫细胞,具备吞噬能力与呼吸爆发产生的活性氧(reactive oxygen species, ROS)杀伤机制,若能将其“定向引导”用于外泌体清除,有望为血管内外泌体的高效去除提供新思路。
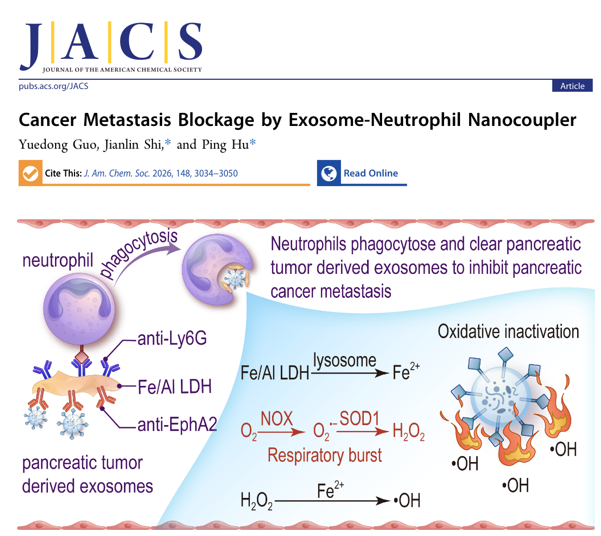
近日,中国科学院上海硅酸盐研究所的施剑林院士团队提出一种“外泌体‑中性粒细胞纳米耦合器”策略,通过将肿瘤外泌体定向锚定至中性粒细胞表面,并利用中性粒细胞内吞与 ROS介导的氧化损伤协同,实现血管内外泌体的失活与清除,从而阻断转移发生。作者以转移潜能极高的胰腺导管腺癌为范例,针对胰腺肿瘤来源外泌体开展验证:以铁/铝层状双氢氧化物(Fe/Al LDH)二维纳米片为基底,采用“修饰‑剥离‑再修饰”实现纳米片两侧不对称功能化——一侧连接靶向中性粒细胞的 Ly6G 抗体,另一侧连接靶向 PTDE 的 EphA2 抗体,使PTDEs被“桥联”并富集到中性粒细胞膜表面。随后,PTDEs可在中性粒细胞吞噬作用下进入吞噬体/溶酶体通路;同时,Fe/Al LDH 促进并增强中性粒细胞呼吸爆发产生 ROS,对外泌体内的肿瘤相关生物分子造成氧化损伤,从而在“捕获‑内吞‑氧化灭活”的多重作用下实现血管内 PTDEs 的高效清除。体内外结果表明,该策略能够降低外周血 PTDEs 负荷并抑制胰腺癌转移,为“以外泌体为关键转移驱动因素的抗转移治疗”提供了新的材料‑免疫协同路径。更重要的是,依托LDH金属离子组成的高度可调性与商业化抗体库的丰富性,该策略有望拓展为多种兼具双靶向识别与离子介导治疗功能的LDH基纳米耦合器平台,凸显了该平台在纳米医学、肿瘤学与感染性疾病治疗中的广阔应用前景及进一步临床转化潜力。
该研究工作以“Cancer Metastasis Blockage by Exosome‑Neutrophil Nanocoupler”为题发表在Journal of the American Chemical Society上(J. Am. Chem. Soc., 2026, 148, 3034–3050)。第一作者为2018级直博生郭跃东(已毕业),通讯作者为施剑林研究员和胡萍研究员。研究工作得到了国家自然科学基金、中国科学院上海分院人才计划、中国科学院青年创新促进会优秀会员项目、上海市生物医药科技支撑项目、上海市青年东方学者项目、上海市优秀学术/技术带头人计划、江苏先进无机材料产业化基金项目、中国博士后创新人才支持计划、中国博士后科学基金以及上海市博士后激励计划等资助和支持。
论文链接:https://doi.org/10.1021/jacs.5c15070

